学科交叉再结硕果--- Nature子刊发表张先正/孙志军团队研究论文
鳞状细胞癌是口腔中最常见的恶性肿瘤,其五年生存率仅有50%左右。虽然口腔鳞癌具有较高的抗原负荷,对PD-1免疫治疗却仅有15-20%的应答率。最近,一些研究报道了共生微生物可以通过调节宿主免疫从而影响肿瘤的疾病进展和治疗效果。在口腔中寄宿着大量的共生微生物,调节口腔菌群有望能够为口腔鳞癌的免疫治疗提供新的思路。
2021年11月8日,武汉大学化学与分子科学学院张先正教授和武汉大学口腔医院孙志军教授团队在Nature Biomedical Engineering上发表了题为 Biomaterial-mediated modulation of oral microbiota synergizes with PD-1 blockade in mice with oral squamous cell carcinoma的研究论文,首次发现了口腔鳞癌中的消化链球菌具有促进免疫并抑制肿瘤的作用,并设计了含银纳米粒子黏膜粘附性水凝胶对口腔菌群调控以提升免疫治疗的效果,为PD-1抗体治疗口腔鳞癌过程中的低应答问题提出了部分解决方案。该工作第一作者为武汉大学化学与分子科学学院郑迪威博士和武汉大学口腔医院邓伟伟博士。

从罹患口腔鳞癌患者的肿瘤组织和癌旁组织中进行微生物分析,发现消化链球菌在肿瘤组织中的水平明显高于癌旁组织。通过回顾患者的预后和肿瘤中消化链球菌含量的水平,发现高的消化链球菌含量与更长的生存期之间有着很强的相关性。研究表明消化链球菌可以通过Nod2通路Toll样受体的途径激活抗肿瘤免疫应答,激活树突细胞,并进一步提高肿瘤内的杀伤性T细胞水平。因此,上调口腔的消化链球菌含量可能为口腔鳞癌的免疫治疗提供很好的辅助。
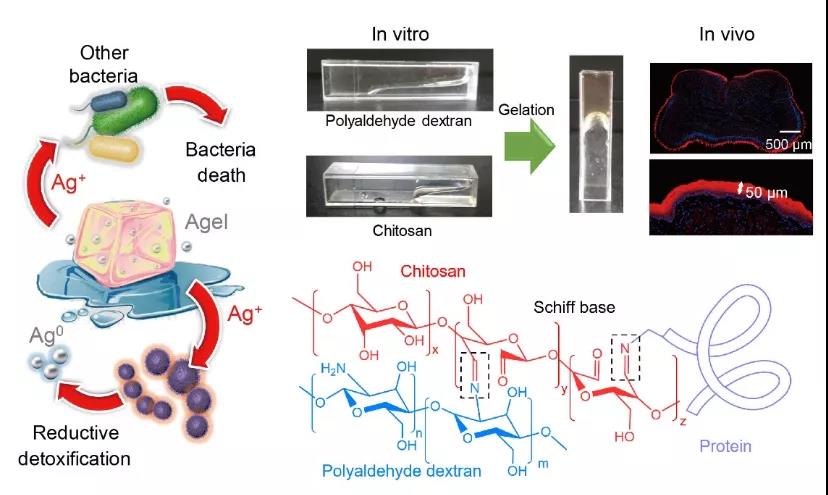
示意图 黏膜粘附性水凝胶调控口腔菌群的作用以及凝胶的黏膜原位形成机制
基于消化链球菌的代谢特征,进一步发现银纳米粒子可以针对性的抑制其他细菌的生长,却对消化链球菌的增殖没有明显抑制作用。这可能是因为消化链球菌缺乏将Ag转化为Ag+的酶,因此无法产生明显的抗菌效果。这一代谢特征使得银纳米粒子可以抑制其他口腔细菌,从而让消化链球菌在口腔环境中获得竞争优势。为了使得银纳米粒子可以稳定的被富集至口腔黏膜处,从而长效调控口腔菌群,进一步构建了黏膜粘附性的水凝胶。通过混合氧化葡聚糖和壳聚糖,醛基和氨基可以快速形成腙键进行交联而形成凝胶。同时凝胶表面多余的醛基可以和组织表面的氨基反应,在小鼠的口腔黏膜表面形成了一层50 μm厚度的薄膜。并可以稳定的在口腔滞留24小时以上,实现长效调控口腔菌群的作用。
在一系列移植有不同消化链球菌水平的唾液的小鼠口腔鳞癌模型中,联合使用水凝胶、消化链球菌以及PD-1抗体均可以产生良好的免疫治疗效果。在4-NQO的诱发口腔肿瘤模型中,预防性的给药也明显抑制了口腔肿瘤的发展。此研究表明调控口腔菌群可能成为提高口腔鳞癌免疫治疗的有效途径,为增强免疫疗法提供新的思路。
近几年来,我院开始探索口腔医学与临床医学、生命医学、化学与分子科学、遥感信息工程学、生物材料科学、物理学等领域深度融合,与相关兄弟学院交流合作,取得积极进展和喜人成绩,此次论文发表在NAT BIOMED ENG(2021年影响因子25.671)是我院又一成果。
互联网和数字化已在众多行业带来颠覆性变革,医疗健康领域也身在其中,发展“新医科”是新时代赋予口腔医(学)院建设世界一流学科的神圣使命。
注:文章来源于BioArt
全文链接:https://rdcu.be/cA1LO